整形外科医がゲノム研究者になる理由 精密医療への道
東京大学 大学院新領域創成科学研究科 松田浩一(最終回)

◇ ◇ ◇
東京大学大学院の松田浩一教授(新領域創成科学研究科メディカルサイエンス群・クリニカルシークエンス分野)は、医療にかかわる研究者であり、また、27万人ものDNAを保管する疾病バイオバンクの運営者だ。さらにいえば、かつて臨床医でもあった。
医学部医学科を出て医師になった松田さんは、どのようにして今の場所に至ったのだろうか。そのあたりを聞いていこう。
「僕の家は、別に父が医者というわけでもないし、特にまわりに医者がいたわけでもないので、医学部に行く強い動機づけがあったわけではないんです。高校時代までに、いろいろ本とか読んだりする中で、医者の仕事はやりがいがありそうだというふうには感じていて、医学部に進学したというのが実際のところです。大学時代はアメリカンフットボール部で、結構怪我をすることが多くて、大学病院の整形外科にお世話になることが多かったのと、5年生になって実習で各科を回り始めた時に整形外科は明るくて楽しい雰囲気で、そういうところに惹かれて整形外科を選びました」
松田さんと話していると、深刻ながんや遺伝性の疾患の話題でも、難しいゲノム解析の話でも、常に楽観的で明るい雰囲気なのだが、一貫して、ものごとの明るい面、楽しい面を見出す性質なのであろうと「腑に落ちる」感覚を抱いた。
「ただ、一般外科のように命に関わる疾患にかかわることへの憧れもあって、整形外科の中ではすごくマイナーな骨軟部腫瘍(こつなんぶしゅうよう)という病気を治療するグループに入りました。骨、筋肉、結合組織などに出来た悪性腫瘍だと思ってください。これが、かなりやっかいで、まず、いろいろな種類がある上に、症例が少ないんです。薬も副作用が強くて、髪が抜けたり、すごく吐き気がしたりするものでした。骨軟部腫瘍のひとつ、骨肉腫の場合ですと、わりと若年の方、当時、20代だった自分から見ても若い10代の患者さんも多くて、そういう方が病気で苦しむのを見ていると、無力感にさいなまれるところがありました。それで、できれば新しい治療法の開発ができないかなというのも考えて大学院に進みたいと思ったんです。これが、がんの領域の研究をするようになった直接のきっかけですね」
松田さんが大学院に入り研究者としてのキャリアをスタートしたのは、1999年のことだ。今でこそ、ゲノム研究と医療は密接にかかわっていると誰もが疑わないが、当時はまだ様相が違った。
「最初はいわゆる分子生物学の基礎研究をしていて、ゲノムについての認識もあんまりありませんでした。特定の分子について詳しく解析するというのが、世間一般の研究のトレンドで、ゲノムを網羅的に見るという発想は、世の中の研究者の間にはなかったと思います。それが2000年にヒトゲノム・プロジェクトでとりあえずゲノムを全部読んだというドラフトが出てきて、ヒトの中にこれだけの数の遺伝子があるんだと分かりました。まずはヒトのゲノムの1セットが分かって、ゲノム全部を対象とした解析ができるツールができてきて、それがRNAレベルであったり、DNAレベルであったり、タンパク質レベルであったりとか、色々なやり方でできるようになってと進んで、僕自身も、アメリカに留学して戻ってきた2004年ぐらいから、ゲノムについての網羅的な研究に携わるようになったんです」

ちなみに、松田さんが留学したテキサス州ヒューストンのベイラー医科大学は、アメリカのトップ医学部・医科大学の一つで、ゲノム医療の最先端の研究から臨床研究まで一貫しててがけている。松田さんは大学院時代はがんを抑制することが知られているp53という遺伝子の、留学時代は骨・軟骨の発生にかかわる分子の研究に従事した。発がんの制御の問題には今回は触れることができなかったが、松田さんは今も引き続きp53を研究対象にしている。「なぜ、細胞ががん化したりしなかったりするのか」ということが解明できれば、がんの予防にも治療にも役立つ知見が得られると期待される分野だ。
そこから先、バイオバンク・ジャパンの試料を用いて、食道がんの全ゲノム関連解析を行った話は前に紹介した。それは、とりもなおさず、その後、世界各地で追従される一大分野の幕開けを告げるものでもあった。
「まあ、お話しする中では、きれいに結果がでたものを話しているわけで、食道がんのものはその最たる例です。実際には、関連する遺伝子が全然見つからなかったこともたくさんあります。うまくいったりいかなかったり、いろいろ積み重ねながら、今やっているっていうところですね」
研究者としての松田さんは、やはり発がんのメカニズムであるとか、あるいは、発がんの抑制のメカニズムであるとか、病気や治療法の背景にある根本の原理的な部分について常に目配りをしているのが、ぼくには印象的だった。個々人に合った予防、検査、医療は、いつでも手持ちの知識で少しずつ進んでいくものだけれど、さらに上のレベルに達するには、やはり原理的な解明が必要なことが多そうだ。

疾病バイオバンクを運営する立場で、今後大きく進展するであろう研究のジャンルはなにかと問うと、松田さんは「ヒューマンノックアウトプロジェクト」と答えた。
耳慣れない言葉だが、「ノックアウトマウス」なら聞いたことがある人も多いのではないだろうか。特定の遺伝子を無効化(ノックアウト)する操作を施されたマウスのことで、その遺伝子の働きを調べるような動物実験で使われる。「ヒューマンノックアウト」はそのヒト版だが、実験のために特定の遺伝子を無効化するのはありえないので、バイオバンクに集積されたDNAデータを活用することになる。
「数十万人のデータが揃ってくると、ある遺伝子が欠けていたり、まったく機能しないような例も出てきます。これは実質的に、その遺伝子をノックアウトした状態ですよね。もしもそれが、1万人に1人ぐらいの非常に頻度が少ないものでも、27万人いればその中で27人はいます。その27人について、どういう病気になりやすかったというような情報を調べることで、ヒトレベルでどの遺伝子がどういう機能を持っており、いろんな表現型、体質とかに関わってくるかというのがおそらく分かってきてます。これまで我々が行ってきたのが、病気の人のゲノムから関係ありそうな遺伝子を見つけていく『順方向(フォワード)の遺伝学』だとしたら、こちらは稀な遺伝子を持っていたり、あるいは持っていない人がどんな病気になりやすいかなどを見ていく『逆方向(リバース)の遺伝学』です」
1万人に1人の変異で特定の遺伝子が働かない人というのは、こういったバイオバンクがないとなかなか見いだせない。ちなみに、本連載で話題にしてきた一塩基多型でも関連する遺伝子が働かなくなることがあるが、それとの違いは、実は頻度だ。「変異」ではなく「多型」と言う場合、その集団で1パーセント以上の割合でみられるものを指す。それよりも稀なものは「変異」として扱われる。1パーセント以上もあるようなものは、変異だとか異常とか言わずに、すでに定着しているヒトの多様性の一部であると理解した方がよい、ということでもある。一方、「多型」ではなく「変異」を見つけたら、それはそのまま新たな研究テーマに直結する。
「逆方向の遺伝学ということで、そういう方々を見つけたら、より詳しく表現型を調べることになります。我々は、臨床情報を5000項目も集めていると言いましたけれど、それでもごくごく限られた範囲のものです。例えば、この遺伝子がインフルエンザに関係するウイルスの感染経路に関係するかもしれないという時に、その人がインフルエンザにかかったかどうか細かい情報までは集めていません。もしくは認知症に関係するかもしれないとすると、その人が認知症になったかどうかとか、いくつで発症したか、例えばその人の病院にアクセスして情報を得れば、データを調べることで様々なことが明らかになっていくはずなんです。場合によっては、本人や家族の方にインタビューをお願いすることもあるかもしれません」
もちろん倫理的な問題はクリアしなければならないのだが、データを集積するということはつまりこういうことだ。
最後に、松田さんが今、試みている、少し方向性の違う新たな展開に触れて本稿を終える。
1999年、研究者に転身してから、ほぼ20年、臨床から離れている松田さんだが、一連のゲノム研究を経て、バイオバンクを運営する立場になりつつも、もう一度、自分自身の研究として、整形外科医時代のテーマに立ち戻っているという。
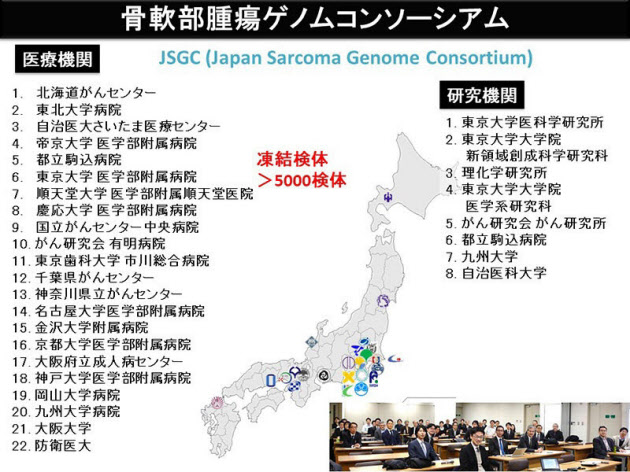
「さきほども言いました骨軟部腫瘍の件です。骨とか筋肉にできるような悪性腫瘍って、悪性腫瘍の中の1%ぐらいですし、発生する場所も種類もすごく細かくて腫瘍の組織型が140種類以上にも分類されているんです。つまり、ひとつひとつの種類の腫瘍の症例がとても少なくて、一番多い骨肉腫でも国内で年間100から150症例くらいです。がんゲノムの解析をするにしても、少なくとも数十程度の献体が必要なので、1つの病院で集めるのは難しくて、今、国内の主要ながんの病院の先生方とネットワークを組んで、骨軟部腫瘍ゲノムコンソーシアムというのを作りました。そして、手始めに、その中の10種類ぐらいの腫瘍についてゲノム研究をやっているところです」
これは、バイオバンク・ジャパンのような大規模な疾病バイオバンクで登録対象になってこなかったような希少疾患にまで、研究の対象が伸びてきたということだ。
「骨軟部腫瘍って本当にマイナーなので、研究費とかも取りにくいですし、薬の開発にしても、たぶん製薬会社とかもそんなに興味がないんですよ。症例が少ない、患者が少ないというのは、解析もしにくいし、研究費も得にくいということです。でも、今は、そういう希少疾患をちゃんと見ていこうという機運が出てきました。このタイプの骨軟部腫瘍には、こういう遺伝子の異常があるとか、まずは基盤となるデータをつくる。がんでいうと、5年ぐらい前にやっていたことを、今ちょっと遅れて始めていて、それが分かった次の段階としては、今後どういう治療をやればいいのか、治療法の選択とか、効果測定に関係することをやっていくことになると思います。この分野でも、精密医療、オーダーメイド医療と呼べるものが、おそらく5年ぐらい先には、実現しているんじゃないかと期待しています」
松田さんの臨床医としての原点と、研究者としてのキャリアが、ぐるりと一周めぐって一致したところだ。たぶん、5年後、10年後、さらに「もう一周」くらいした時には、ぼくたちはきっと精密医療だとか、オーダーメイド医療といった言葉を使うこともなく、むしろ当たり前のこととして享受しているかもしれない。松田さんと話していて、そんな楽観的な未来を思い描くことができた。
=文 川端裕人、写真 内海裕之
(ナショナル ジオグラフィック日本版サイトで2019年1月に公開された記事を転載)
1969年、大阪生まれ。東京大学 大学院新領域創成科学研究科 メディカル情報生命専攻 クリニカルシークエンス分野 教授。M.D., Ph.D. 1994年、東京大学医学部医学科卒業後、整形外科医の勤務経験を積んだのち、基礎研究を志して1999年、東京大学大学院医学系研究科外科学専攻に入学。2003年に米国ベイラー医科大学研究員になり、博士号も取得。2004年、東京大学医科学研究所、ヒトゲノム解析センター助手に就任。2009年に准教授になり、2015年より現職。
1964年、兵庫県明石市生まれ。千葉県千葉市育ち。文筆家。小説作品に、肺炎を起こす謎の感染症に立ち向かうフィールド疫学者の活躍を描いた『エピデミック』(BOOK☆WALKER)、夏休みに少年たちが川を舞台に冒険を繰り広げる『川の名前』(ハヤカワ文庫JA)、NHKでアニメ化された「銀河へキックオフ」の原作『銀河のワールドカップ』(集英社文庫)とその"サイドB"としてブラインドサッカーの世界を描いた『太陽ときみの声』『風に乗って、跳べ 太陽ときみの声』(朝日学生新聞社)など。
本連載からのスピンアウトである、ホモ・サピエンス以前のアジアの人類史に関する最新の知見をまとめた『我々はなぜ我々だけなのか アジアから消えた多様な「人類」たち』(講談社ブルーバックス)で、第34回講談社科学出版賞と科学ジャーナリスト賞2018を受賞。ほかに「睡眠学」の回に書き下ろしと修正を加えてまとめた『8時間睡眠のウソ。 日本人の眠り、8つの新常識』(集英社文庫)、宇宙論研究の最前線で活躍する天文学者小松英一郎氏との共著『宇宙の始まり、そして終わり』(日経プレミアシリーズ)もある。近著は、「マイクロプラスチック汚染」「雲の科学」「サメの生態」などの研究室訪問を加筆修正した『科学の最前線を切りひらく!』(ちくまプリマー新書)
ブログ「カワバタヒロトのブログ」。ツイッターアカウント@Rsider。有料メルマガ「秘密基地からハッシン!」を配信中。
ワークスタイルや暮らし・家計管理に役立つノウハウなどをまとめています。
※ NIKKEI STYLE は2023年にリニューアルしました。これまでに公開したコンテンツのほとんどは日経電子版などで引き続きご覧いただけます。
関連企業・業界


















