回復者の血液でコロナ治療 米で承認、その「実力」は
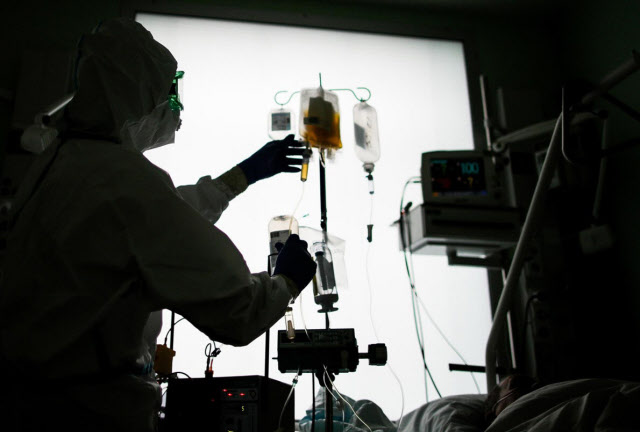
米国のドナルド・トランプ大統領は、新型コロナウイルスの治療法とワクチンで進展が見られないことで食品医薬品局(FDA)を非難したが、その翌日の2020年8月23日に一転、新型コロナへの回復期血漿(けっしょう)療法をFDAが緊急承認したと発表した。
血漿とは、血液から赤血球などの血球成分を取り除いたもので、さまざまな抗体が含まれる。そこで、感染症から回復した者の回復期血漿を患者に投与して、病原体の撃退に役立てるのがこの治療法のねらいだ。1918年のスペインかぜ以来、医師たちはこうしたやり方で感染症と闘ってきた。
だが、新型コロナの回復期血漿療法に関しては、もう何カ月も前から世界で70以上の臨床研究が行われているにも関わらず、重症患者への有効性はいまだに確認されていない。そんななか、トランプ大統領の発表により、これにまつわるあるひとつの研究が、医学界と政界の激しい論争に巻き込まれようとしている。
FDAの決定は、主に米ミネソタ州ロチェスターにあるメイヨー・クリニックが8月に発表した臨床試験の暫定的な結果に基づいている。それによると、入院から3日以内に血漿療法を受けた患者の死亡率が、3.2%低下したという。ただし、この論文はまだ専門家による査読を受けていない。
血漿療法の治験には数百万ドルの連邦予算が投じられ、何万という患者を対象に実施されているが、大きな欠陥がひとつある。試験には、効果を比較する対照群、つまり血漿療法を受けない患者のグループが存在していないことだ。それが、試験結果の解釈を困難にしている。
「まだ最終的な結論には程遠いということを、研究機関にも個人にも認識してほしいと思います」と、オハイオ州にあるクリーブランド・クリニックの呼吸器科医ダニエル・カルバー氏は話す。血漿療法の研究は全体的には見込みがあるものの、今回のFDAによる緊急承認が正式な承認と同等と見なされて、患者や医師がまだ有効性の確認されていない治療法に走ってしまうことを、カルバー氏は懸念している。
「人道的な使用」が行き過ぎる弊害
メイヨー・クリニックのプロジェクトは、全米の医師の地道な努力から生まれた。医師たちは、新型コロナ感染症の治療に回復期血漿療法を適用する筋道を2通り思い描いていた。ひとつは十分に吟味された臨床試験。そしてもうひとつは、命に関わる重症患者へ例外的に未承認薬を投与する「コンパッショネートユース(人道的使用)」だ(編注:日本ではコンパッショネートユースは治験の一環とされ、「人道的見地から実施される治験」「拡大治験」とも呼ばれる)。
ところが今、このコンパッショネートユースが当初の期待以上に大きくなりすぎて、臨床試験が二の次になろうとしている。予算やインフラの不足で、臨床試験は開始当初から後れを取っていた。
「私の経験から言えるのは、現時点で、すみやかに治験を開始できる態勢は整っていないということです」と、ニューヨーク市のアルバート・アインシュタイン医科大学感染症学部長で抗体の専門家であるリーズアン・ピロフスキー氏は言う。「治験の実施計画書がないわけでも、積極的に取り組もうという研究者や患者がいなかったわけでもありません。ただ、資金と組織化された監督機能が欠けていました」
「WIRED」の8月21日付の記事によると、米国でのコンパッショネートユースは急速に拡大し、2700以上の病院で実施されているが、そのうちの一部は臨床試験の十分な仕組みもノウハウも持ち合わせていないという。メイヨー・クリニックだけでも、入院患者への回復期血漿の使用に保健福祉省から4800万ドル(約50億円)の予算を受けていた。
「あまりの人気ぶりに、魔法の治療薬という印象を与えてしまっていますが、それは正確ではありません。全ての非無作為化試験で期待できる兆候がみられるものの、まだ自信をもって効果があるとは言えない、というのが現状です」と、米ニューヨーク大学ランゴーン医療センターの感染症の専門家ミラ・オルティゴーザ氏は話す。
本来であれば、大規模な治験を行い、無作為に分けられた被験者が本物の治療薬かプラセボ(偽薬)のどちらかを投与されてその結果を比較する。だが今のところ、世界では治験の規模が小さいか、あるいはメイヨー・クリニックのように対照群のない観察研究しか行われていない。対照群なしには、患者が自力で回復したのか、血漿なしでも結果は同じだったのかを知ることはできない。
「率直に言って、回復期血漿療法を受けた数万人の患者が、それによって回復したのか、悪くなったのか、それとも全く変わらなかったのか、最終的に判断のしようがありません」と、英国の治験を率いる1人である英オックスフォード大学心臓学教授のマーティン・ランドレー氏は言う。
7月30日、メイヨー・クリニックのマイケル・ジョイナー氏の研究チームは、査読前の論文を公開するサイト「MedRxiv」に複数の小規模治験の結果をまとめた総説論文を投稿し、新型コロナ患者への回復期血漿療法の有効性が示唆されると結論付けた。FDAも、同じ治験と研究、そしてより広範囲なメイヨー・クリニックのコンパッショネートユースの結果を引用して、緊急承認を決定したとしている。総説の共同著者であるピロフスキー氏は、FDAに対するあからさまな圧力はあったものの、承認の決定は正当であると言う。
「私は科学とデータを信用し、FDAによる決定も同じく科学とデータに基づいていると信じるに足る理由があります。今回はただ、本当に残念なことが重なってしまいました」
無作為化比較試験によってのみ評価
FDAの緊急承認は、正式な承認とは異なる。新型コロナに関して、FDAから正式な承認を受けた治療法は米国にはまだ存在しない。FDAは、次のような声明を発表している。「現在入手可能な証拠に基づけば、回復期血漿療法を新型コロナの新たな標準治療とすることはまだできない。しかし、既知の潜在的な利益がリスクを上回る(編注:コンパッショネートユース実施条件のひとつ)と結論付けることは妥当である」
科学者たちのなかには、トランプ大統領が数カ月後に迫る大統領選前に承認を急がせようとFDAに圧力をかけたのではと疑う声がある。回復期血漿療法だけでなく、大統領は今は効果が否定されたヒドロキシクロロキンも強く推していた。
8月23日、英フィナンシャル・タイムズ紙の米国版は、トランプ政権がこの秋にワクチンの早期承認を検討していると報じたが、それまでに大規模な臨床試験が終了することはまずありえない。ロイターは8月20日、有効性が実証されていないワクチンをFDAが早期承認するようなことになれば辞任すると、FDAのある高官が話していると報じた。連邦政府は既に、国民に血漿の寄付を求めるデジタル広告とラジオ広告に800万ドル(約8億4000万円)の予算を組んでいる。
米アリゾナ大学の研究者で集中治療室医長のクリスチャン・バイム氏は、血漿療法に関わっている科学者たちを信頼しているため、政治的圧力のことは心配していないと語る。
「科学者たちが正しいことをしてくれると信じています。最良の慣例に従わない結果起こりうるリスクは、彼らにとってあまりにも大きすぎます」。ナショナル ジオグラフィックへのメールで、バイム氏はそう警告した。
回復期血漿療法をめぐる混乱は、新型コロナへの対応でことごとくつまずいてきた米国の問題のひとつを浮き彫りにした。それは、臨床試験の過程が全国的に連携されていないことだ。
ピロフスキー氏が率いる回復期血漿の無作為化比較試験(RCT)は、これまでに190人の被験者を集めている。4月17日にニューヨーク市で治験を開始したときには、連邦政府からの予算は受けていなかった。それから数週間のうちにニューヨーク市ではコロナが収束し始め、患者が集められなくなった。そして最近になってようやく国立衛生研究所から予算が回ってきたため、現在治験はコネチカット州、フロリダ州、テキサス州に拡大されている。「追いかけっこのような状態でした」と、ピロフスキー氏は振り返る。
ナショナル ジオグラフィックがインタビューした医師たちは、有効性を確認する無作為化比較試験の結果を見極めたいと答えた。
「人間の血漿を使用することには、理論上のリスクも現実的なリスクもあります。また、適切に評価されていないため、抗体が十分に含まれない血漿によるリスクも考えられます。それらのリスクは全て、無作為化比較試験によってのみ評価できるものです」と、カルバー氏は言う。
(文 MICHAEL GRESHKO、訳 ルーバー荒井ハンナ、日経ナショナル ジオグラフィック社)
[ナショナル ジオグラフィック 2020年8月26日付の記事を再構成]
ワークスタイルや暮らし・家計管理に役立つノウハウなどをまとめています。
※ NIKKEI STYLE は2023年にリニューアルしました。これまでに公開したコンテンツのほとんどは日経電子版などで引き続きご覧いただけます。